Name: Kilian Wessel
Die Atombindung
Einzelne Wasserstoffatome
Das Wasserstoffatom besitzt nur ein Elektron. Seine negative Ladung ist über den ganzen Raum verteilt. Man spricht deshalb von einer sogennanten Elektronenwolke. Dabei handelt es sich jedoch nur um ein Elektron.
Bindung eines Wasserstoffmoleküls
Wenn sich zwei Wasserstoffatome nähern, so durchdringen sie ihre Elektronenwolken. Die Stärke der Durchdringung hängt hierbei von dem Abstand zwischen den Atomkernen ab: Ist der Abstand zwischen den Atomkernen kleiner, so ist die Durchdrinung stärker.
Die Elektronen befinden sich nun zwischen den beiden Kernen.
Außerdem entsteht eine gemeinsame Elektronenwolke um beide Atomkerne. Dort befinden sich zwei Elektronen. Durch diese Elektronenwolke, werden die Wasserstoffatome zusammengehalten und bilden ein Wasserstoffmolekül. Diese Bindung nennt man Atombindung.
Bindungsenergie
Wenn ein Wasserstoffmolekül gebildet wird, so wird Energie frei. Diese Energie nennt man Bindungsenergie. Will man die Atome wieder trennen, so wird die selbe Energie benötigt. Ein Wasserstoffmolekül ist stabiler als die beiden einzelnen Wasserstoffatome.
Valenzstrichformel
Die Valenzstrichformel wird oft verwendet, um die Moleküle darzustellen. Hierbei werden alle Elektronenpaare dargestellt (bindende und nicht bindende). Will man die Valenzstrichformel aufstellen, so sind folgende Regeln zu beachten:
- Zunächst schreibt man die Elementsymbole der Atome auf.
- Danach werden alle Valenzelektronen der einzelnen Atome gezeichnet. Man denkt sich nun vier Elektronenwolken, die zunächst mit je einem Elektron besetzt sind und -wenn nötig- danach mit je noch einem Elektron besetzt werden können. Wichtig hierbei ist, dass eine Elektronenwolke maximal zwei Elektronen besitzen kann.
Beispiel: Das Fluoratom (F) hat ein einzelnes Valenzelektron und drei Valenzelektronenpaare.
Ausnahme: Das Heliumatom (HE) steht in der VIII. Hauptgruppe, hat jedoch nur zwei Valenzelektronen, also ein Elektronenpaar.
- Jetzt wird das Molekül gebildet. Um dies zu machen, werden je zwei einzelne Valenzelektronen zu einem bindenden Elektronenpaar gepaart. Die bindende Elektronen Paare stehen dann zwischen den beiden bindenden Atomen.
Beispiel: H-H
Die überbleibenden Elektronenpaare bezeichnet man als nicht bindende Elektronenpaare.
Mehrfachbindungen
Eine Mehrfachbindung ist eine Elektronenpaarbindung, bei der zwei Atome nicht nur durch ein Elektronenpaar verbunden sind, sondern durch mehrere.
Die polare Atombindung
Die Bindung im Hydrogenchloridmolekül
Da sich die Elemente Chlor und Wasserstoff in ihrer Elektronegativität unterscheiden (Chlor = relativ hohe Elektronegativität [EN(Cl) = 3,0] / Wasserstoff = geringere Elektronegativität [EN(H) = 2,1]), werden die Bindungselektronen vom Chloratom stärker angezogen. Darauf folgt, dass das Chloratom einen Überschuss an negative Ladung besitzt. Dadurch hat das Wasserstoffatom einen Mangel an negativer Ladung, sodass die positive Ladung seines Atomkerns überwiegt. Folglich hat das Hydrogenchloridmolekül einen "Pluspol" sowie einen "Minuspol"
=> Dipolmolekül
Eine polare Atombindung liegt also dann vor, wenn in einem Molekül Atome verschiedener Elektronegativität verbunden sind.
Polarität der Bindung
Die Elektronegativitätsdifferenz zwischen den beiden Atomen gibt an, wie groß die Polarität der Bindung ist. Je größer die Elektronegativitätsdifferenz, desto größer die Polarität der Bindung.
Der räumliche Bau von Molekülen
VSEPR-Modell
Das VSEPR-Modell (VSEPR ist die Abkürzung für englisch valence shell electron pair repulsion, deutsch Valenzschalen-Elektronenpaar-Abstoßung), auch EPA-Modell (Elektronenpaarabstoßungsmodell) oder ursprünglich auch VEPR-Theorie (englisch valence electron pair repulsion theory), führt die räumliche Gestalt eines Moleküls auf die abstoßenden Kräfte zwischen den Elektronenpaaren der Valenzschale zurück.
Hier sind einige Beispiele:
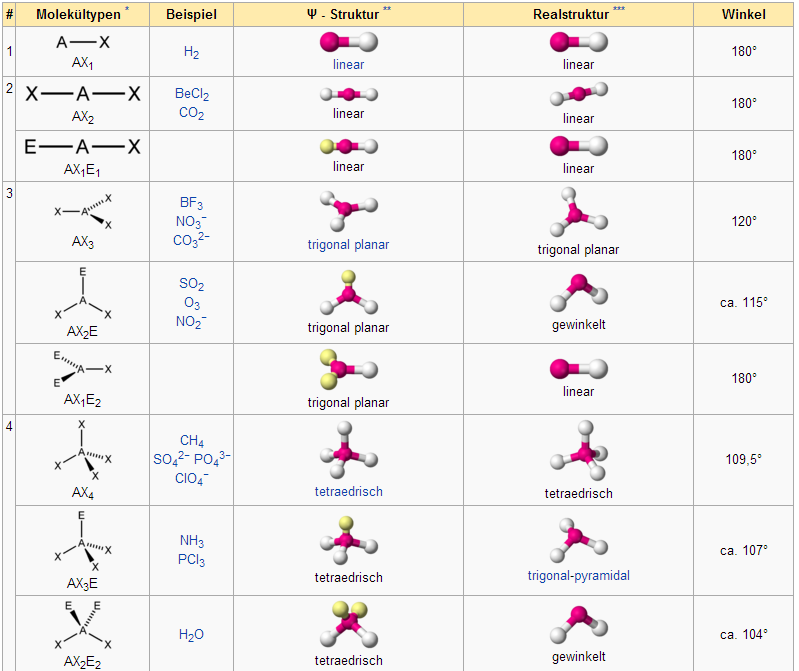
Molekültypen und Molekülgeometrie (Klicken zum Vergrößern)
Quelle: Public domain: http://de.wikipedia.org/wiki/VSEPR-Modell, Mehrere Autoren
Es werden nicht nur die bindenden Elektronenpaare berücksichtigt, sondern auch die nicht bindenden Elektronenpaare.
