Name: Sascha Firmenich, 2012 , Lucas Röder 2021-06
Aufbau der Aminosäuren
Die Aminosäuren gehören zu der chemischen Klasse der organischen Verbindungen. Sie zeigen einen einheitlichen Aufbau:
Es gibt immer ein zentrales Kohlenstoffatom, auch alpha- Kohlenstoffatom, genannt. An diesem bindet jeweils eine Carboxylgruppe - COOH und eine Aminogruppe - NH2, ein Wasserstoffatom - H, und auch ein sogenannter Rest - R.
Dieser Rest ist von entscheidender Bedeutung für die Aminosäure. Er wird auch als Seitenkette bezeichnet und ist charakteristisch für die jeweilige spezifische Aminosäure.
Die Grundstruktur lautet somit: 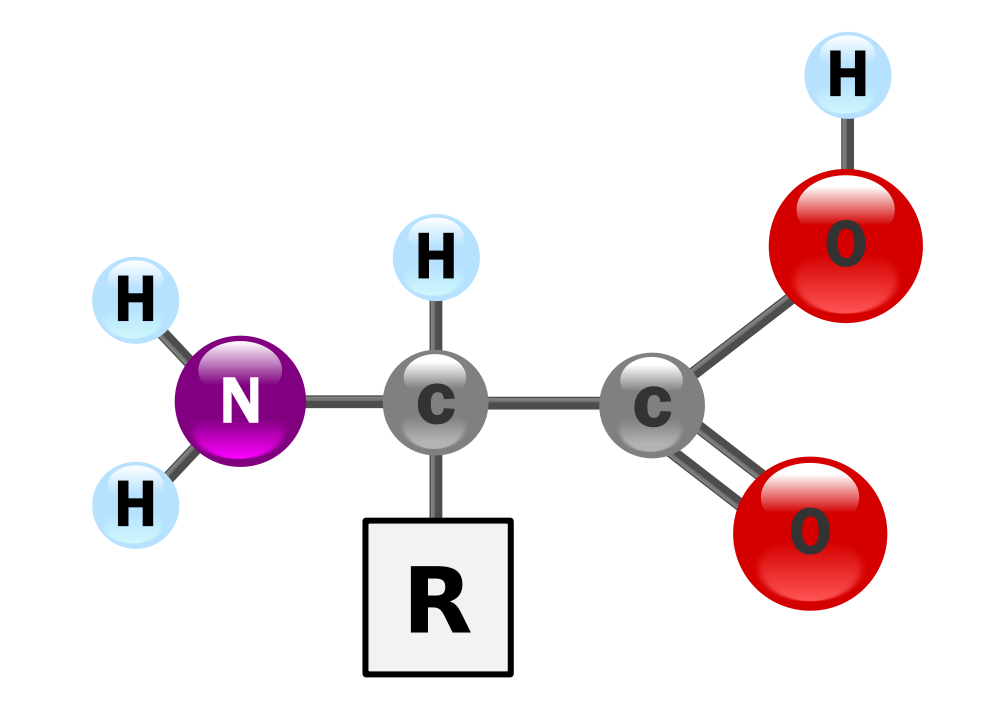
Quelle Bild: Yassine Mrabet, Public Domain, http://commons.wikimedia.org/wiki/File:AminoAcidball.svg
Es kommt also auf die Atomgruppen (funktionellen Gruppen) an, die sich in der Restgruppe befinden und somit die verschiedenen Aminosäuren definieren.
Besteht die Restgruppe nur aus einem Wasserstoffatom, so entsteht die einfachste Aminosäure Glycerin (Gly).
Außerdem differenzieren sich die Seitenketten der Aminosäuren durch ihre Säure- Base- Reaktion, durch ihre Polarität und durch ihre Ladung.
Beispiel einer unpolaren Aminosäure:
Glycin (Gly)
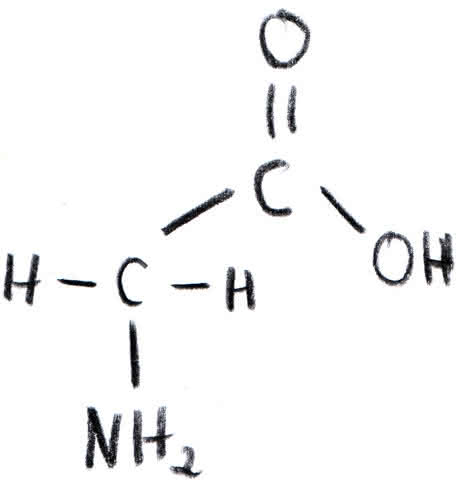
Beispiel einer polaren Aminosäure:
Cystein (Cys)
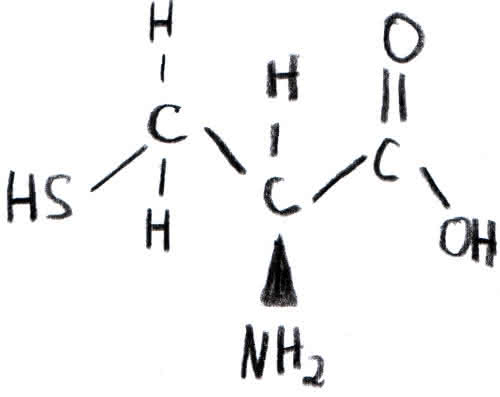
Beispiel einer elektrisch geladenen Aminosäure:
Asparaginsäure (Asp) 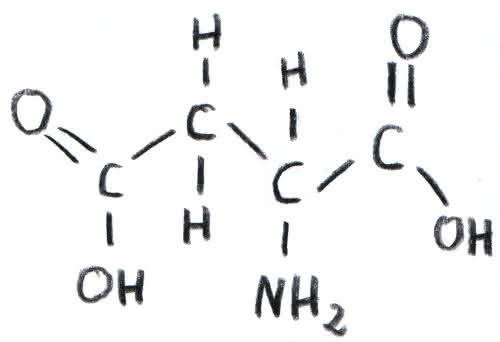
Ist die Asparaginsäure elektrisch geladen, so liegt die -COOH Gruppe in der Form eines COO- - Ions vor.
Säure-Base-Reaktion:
- in neutraler, wässriger Lösung und als Feststoff liegen Aminosäuren als Zwitterionen vor, d. h. die Aminogruppe ist protoniert(basisch)
und die Carboxylgruppe ist deprotoniert(sauer):
H3N+ - CHR - COO-
-die Aminogruppe wirkt als Base, da sie ein Proton aufnimmt (Protonenakzeptor) und
die Carboxylgruppe wirkt als Säure, da sie ein Proton abgibt (Protonendonator).
Die Titration der Aminosäuren:
H3N+ - CHR- COOH = H3N+ - CHR - COO- = H2N - CHR - COO-
- wenn der Aminosäurerest R ebenfalls titrierbar, ist so muss er in der Gleichung mit berücksichtigt werden
Die Nettoladung der Aminosäure ist vom pH-Wert abhängig, bei einem bestimmten pH-Wert ist die Nettogleichung gleich null (Ladungsgleichgewicht -> Zwitterion).
Der entsprechende pH-Wert wird als isoelektrischer Punkt bzw. als pI der Aminosäure bezeichnet und ist für jede Aminosäure spezifisch bzw. charakteristisch.
Säure-Base-Verhalten:
Das Verhalten des Aminosäurerestes R beeinflusst das Säure-Base-Verhalten proteinogener Aminosäuren entscheidend (besonders bei der Betrachtung von Proteinen), weil die NH2- und COOH-Gruppen in Proteinen aufgrund der Peptidbindung nicht titrierbar und damit ungeladen sind und es somit auf das Verhalten des Rests R ankommt.
Das Verhalten der Seitenkette R hängt von ihrer Konstitution ab, d. h., ob die Seitenkette selbst wieder als Protonenakzeptor oder -donator wirken kann. Folglich werden die proteinogenen Aminosäuren in basische und saure Aminosäuren eingeteilt.
Zu den basischen Aminosäuren gehören:
Lysin
Arginin
Histidin
Zu den sauren Aminosäuren gehören:
Asparaginsäure (Aspartat)
Glutaminsäure (Glutamat)
Weitere Aminosäuren mit ionisierbaren Resten:
Cystein
Tyrosin
Die Reste R der hier genannten Aminosäuren werden auch als titrierbare Reste bezeichnet.
Die Reste R der anderen proteinogenen Aminosäuren sind unter physiologischen Bedingungen nicht ionisierbar und wirken daher weder als Base noch als Säure.
Der pK-Wert ist der pH-Wert, bei der die titrierbaren Gruppen zu gleichen Teilen protoniert und deprotoniert vorliegen.
D. h., die titrierbare Gruppe liegt zu gleichen Teilen in ihrer basischen, wie in ihrer sauren Form vor (siehe: Henderson-Hasselbalch-Gleichung).
Meistens spricht man statt vom pKS vom pK, d. h. vom pK der Säure.
In diesem Sinne müsste allerdings vom pK des Lysins als pKB, d.h. vom pK der Base gesprochen werden.
Aus Gründen der Vereinfachung wird diese Notation aber allgemein weggelassen, da sie sich auch aus dem Sinnzusammenhang selbst ergibt (d. h. ob die Gruppe als Base oder Säure wirkt).
Der pK ist keine Konstante, sondern hängt von der Temperatur, der Ionenstärke und der unmittelbaren Umgebung der titrierbaren Gruppe ab und kann daher stark schwanken.
Ist der pH höher als der pK einer titrierbaren Gruppe,
so liegt die tirierbare Gruppe in ihrer basichen (deprotonierten) Form vor.
Ist der pH jedoch niedriger als der pK der titrierbaren Gruppe, so liegt die titrierbare Gruppe in ihrer sauren (protonierten) Form vor:
für z.B Asp (pK = 3,86) bei pH 7:-> die Seitenkette liegt nahezu vollständig in ihrer deprotonierten Form vor
für z:B Lys (pK = 10,53) bei pH 7:-> die Seitenkette liegt nahezu vollständig in ihrer protonierten Form vor
Die Seitenketten basischer Aminosäuren sind in ihrer protonierten (sauren) Form einfach
positiv geladen und in ihrer deprotonierten (basichen) Form ungeladen.
Die Seitenketten der sauren Aminosäuren (einschließlich Cystein und Tyrosin) sind
in ihrer protonierten (sauren) Form ungeladen und in ihrer deprotonierten (basischen)
Form einfach negativ geladen. Deswegen spielt der pH-Wert für die Eigenschaften der Seitenkette
eine so wichtige Rolle, da sich das Verhalten der Seitenkette verändert,
wenn sie geladen bzw. ungeladen ist.
Auswirkungen auf die Löslichkeit der Aminosäure
Die titrierbaren Seitenketten beeinflussen das Löslichkeitsverhalten
der entsprechenden Aminosäure. In polaren Lösungsmitteln gilt: geladene Seitenketten
machen die Aminosäure löslicher, ungeladene Seitenketten machen die Aminosäure unlöslicher.
In Proteinen kann das dazu führen, das bestimmte Abschnitte hydrophiler oder hydrophober werden,
wodurch die Faltung und damit die Aktivität von Enzymen vom pH-Wert abhängt.
Mit stark sauren und basischen Lösungen können Proteine deswegen auch denaturiert werden.
Verschiedene Aminosäuren können zu unterschiedlich langen Ketten verbunden werden, indem die Aminogruppe einer Aminosäure mit der Carboxylgruppe einer anderen Aminosäure reagiert und unter Abspaltung von Wasser eine Peptidbindung bildet.
Die Peptidbindung der Aminosäuren ist das grundlegende Bauprinzip zur Entstehung aller Proteine.
