Namen: Lucas, Kübra, Franziska, Nina, Namen: Christopher, Gabriel, Mandana und Evelyn (alle 2013, 10L1)
Lara 2019-12
Vorkommen von Eisen:
- nie elementar in der Natur (außer in Meteoriten)
- Hauptbestandteil (zusammen mit mit Nickel) im Erdkern
- 28,8% des Gesamtanteils der Erde
- 4. häufigstes Element
- ca. 4,7% in der Erdkruste
- wirtschaftlich bedeutend: Hämatit, Magnetit, Siderit, Brauneisenstein, Pyrit
- größte Eisenerzlieferanten: Brasilien, Australien, China, Russland, Indien,USA,Kanada,Schweden,Frankreich
- Erdkern besteht hauptsächlich aus Eisen
- wichtiger Mineralstoff im Körper
- Spurenelement -> erforderlich für den Stoffwechsel
- wird im Blut aufgenommen
- ca. 60% in Hämoglobin (roter Blutfarbstoff)
- Stärkung des Immunsystems
- ca. 10% des Eisens in Lebensmitteln können aufgenommen werden
- im Blut wird es mit Transferrin* transportier zu Muskeln, Knochenmark, Leber &,
- Milz, des Weiteren ist es wichtig für die Bildung einiger Enzyme (hauptsächlich in der Leber gebildetes Eisentransportmittel)
- industriell heißt es auch Gusseisen.
- Stahl wird nicht als Eisen bezeichnet, sondern als Eisenmetall.
Eisen und Nickel bilden den Hauptbestandteil des Erdkerns. Raseneisenstein (hohe, eisenhaltige Verfestigung) und offenliegende Erze wurden als erstes abgebaut. Heute findet der Abbau von 40-prozentigem Magneteisenerz statt. Die Reinform des Eisens ist in der Natur nur selten vorfindbar. Diese Naturform Eisens ist an 120 Orten zu finden. Häufig findet man jedoch Eisenerz. Man kennt circa 1500 Eisenminerale.
Eisengewinnung
Erzgewinnung und –aufbereitung
Eisenerz wird sowohl im Tage als auch in Tiefbau gefördert, wobei die Gewinnung beim Tagebau weitaus effektiver und kostengünstiger ist und so häufiger genutzt wird. Insbesondere in Südamerika, China, Osteuropa und Kanada wird heute im Tagebau Erz gefördert.
In der Regel muss zu feines Eisenerz, bevor man es weiterverarbeiten kann, in einer Sinteranlage zu Sinter verarbeitet werden. Dabei wird das Erz unter erhöhtem Druck erhitzt und so gepresst, es verschwinden Poren und aus kleineren Bruchstücken werden feste aber spröde Brocken gepresst. Neben dem Sintern von Bruchstücken wird feiner Erzstaub durch die Zugabe von Wasser und Bindemitteln wie beispielsweise Sand oder Kalk bei gehobenen Temperaturen der Staub gebunden und zu Pellets verarbeitet.
Dies ist notwendig, damit in der späteren Weiterverarbeitung im Hochofen beim Einschmelzen gegebenenfalls vorhandener Staub oder Erzbruchstücke nicht die Luftzufuhr behindern oder unterbrechen.
Einschmelzen im Hochofen
Die Produktion von Eisen findet in Hochöfen (Anlage zur Gewinnung von Eisen durch Reduktion von Eisenoxid) statt, kann jedoch auch ohne diese vollzogen werden. Man kann Eisen sowohl mit Kalkstein, als auch mit Koksgrus und Wasser vermischen und sintern (Eisenerze werden in Sinteranlagen zusammengebacken).
Bei einem Hochofen handelt es sich um einen Schachtofen bei dem das Eisenerz und das Steinkohlekoks abwechselnd von oben in die Brennkammer eingeführt werden. Diese Rohmaterialien sinken im Ofen ab und erhitzen sich dabei auf bis zu ca. 1800°C, wobei das Eisenoxid schmilzt und der Kohlenstoff aus der Kohle sich mit dem austretenden Sauerstoff aufgrund der anhaltenden Zugabe von 2000°C heißem Stickstoff und Kohlenmonoxid verbindet. Aufgrund von verschiedenen Verschmutzungen der Kohle sowie dem Erz entstehen Abgase, die neben den Prozessgasen Stickstoff und Kohlenmonoxid auch u.a. Siliziumdioxid enthalten.
Nach ca. 8 Stunden ist die Reduktion und die Schmelze abgeschlossen und aus dem Ofen kann das ca. 1450°C heiße Roheisen sowie ein weiteres Abfallprodukt, die Schlacke, entnommen werden. Zusätzlich zur gesonderten Entsorgung der Schlacke, da diese einige Schwermetalle enthält, müssen die Abgase in einem aufwändigen Filterprozess gereinigt und vom entstandenen Feinstaub befreit werden.
Das entstandene Roheisen hat einen Eisenanteil von ca. 95%, was für die meisten Stahlsorten zu niedrig ist, da durch den hohen Kohlenstoffrestanteil die Stahlqualität schlechter und der Stahl porös wird.
Neben dem schmelzen des Stahls im Hochofen gibt es noch weitere Möglichkeiten des Einschmelzens, wie beispielsweise die Eisenerzeugung im Schachtofen oder der Erzeugung in der Retorte. All diese Möglichkeiten wurden entwickelt um ungünstige Rohstoff- oder Energiebedingungen auszugleichen. Allerdings ist die Eisenerzeugung durch den Hochofen die wirtschaftlichste und effizienteste, weshalb man in der Industriellen Erzeugung nahezu ausschließlich diese antrifft.
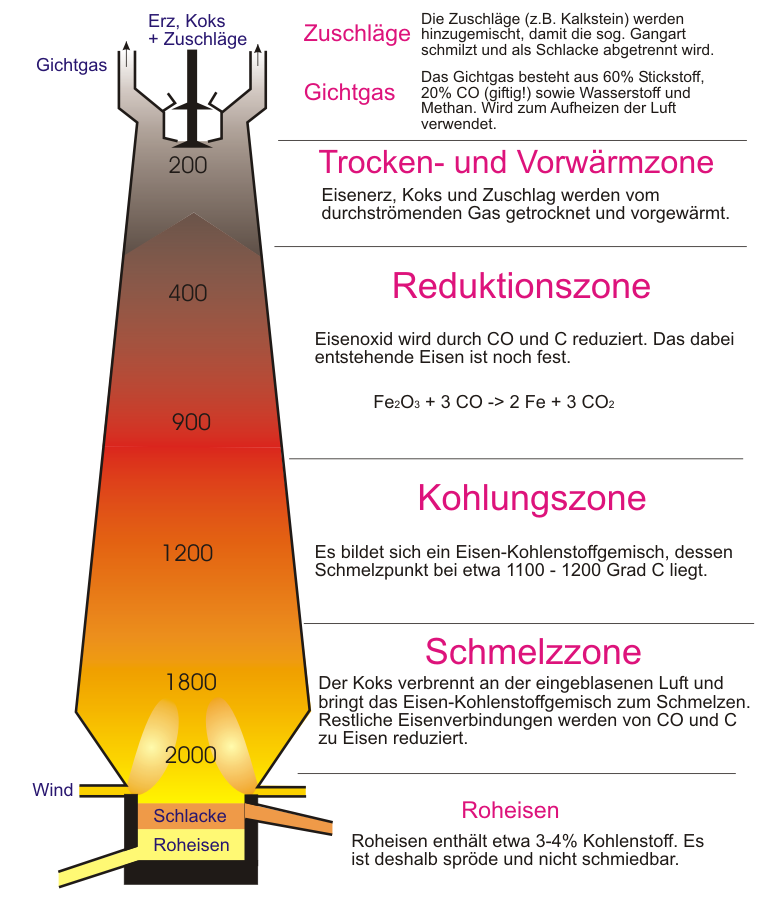
Schematischer Aufbau des Hochofens (Klicken zum Vergrößern)
Quelle Bild: http://commons.wikimedia.org/wiki/File:Hochofenprozess.PNGby Andreas Schmidt
Creative Commons Attribution-Share Alike 3.0 Unported license GNU Free Documentation License, Version 1.2
Eigenschaften von Eisen:
- chemisches Element mit Elementsymbol: Fe
- silbrig-weißes Aussehen
- weiches, dehnbares Metall
- unedles Metall
- Aggregatzustand normalerweise fest
- Ordnungszahl 26 (=> 26 Protonen, 26 Elektronen)
- Molmasse 55,85 g mol
- Elektrisch leitfähig
- Nicht brennbar
- Sehr gute Wärmeleitfähigkeit (z.B : Gußeiserne Pfanne)
- Geruch- und geschmacklos (der typische mit Eisen verbundene Geruch, entsteht durch eine chemische Reaktion bei der Berührung von Eisen mit den Fetten und dem Schweiß der Haut)
- 8. Hauptgruppe (Eisen-Platingruppe; Eisengruppe)
- 4 besetzte Elektronenschalen mit 8 Außeneletktronen
- oxidiert an feuchter Luft
- Elektronegativität: 1,83
- Dichte: 7,874g/cm3
- Schmelzpunkt: 1538°C
- Siedepunkt: 2861°C
- Atommasse: 55,845u
- Zählt zu den Übergangsmetallen
- Oxide: FeO; Fe2O3; Fe3O4
Isotope des Eisens:
- Eisen besitzt 27 Isotope und zwei Kerisomere.
- Vier Isotope sind natürlich und stabil (54Fe, 56Fe, 57Fe, 58Fe)
- 60Fe hat eine Halbwertzeit von 2,62 Mio. Jahren.
- "Äußere" Eigenschaften:
• Aussehen: metallisch glänzend; gräulich
• hartes, dehnbares Schwermetall
• Geruch: geruchlos (reines Eisen). Der bekannte Eisengeruch kommt von der Reaktion von Stoffen des Schweißes und Fettes der Haut mit den dabei entstehenden Eisenionen. Dabei ist der wichtigste Duftträger 1.Octon-3-on, das einen pilzig-metallischen Geruch hervorruft. Die Vorstufe sind die Lipidperoxide, die dadurch entstehen, dass das Hautfett durch bestimmte Enzyme oxidiert wird. Danach werden diese durch die zweiwertigen Eisenionen zersetzt und so werden Duftstoffe frei.
Reaktionsverhalten von Eisen und seinen Verbindungen:
- reaktionsfreudig
- beständig an trockener Luft, in trockenem Chlor, in konzentrierter Schwefel- und Salpetersäure und basischen Agenzien (außer heißer Natronlauge) mit einem pH- Wert über neun.
- in Salzsäure, Schwefelsäure und Salpetersäurelöst es sich rasch. Dabei entwickelt sich Wasserstoff.
- An feuchter Luft oder Wasser, in denen Sauerstoff oder Kohlenstoffdioxid vorhanden ist, wird es unter Bildung von Eisenhydrat (Rost) oxidiert.
- An trockner Luft erhitzt: Bildung einer dünnen Eisen (2,3)-Oxid.
- Stahlwolle reagiert in feuchtem Chlor- Gas: Bildung von brauen Eisen(III)- Chlorid.
- Gemisch von Eisen und Schwefel (Gewichtsverhältnis 7:4) erhitzt: Bildung von Eisen(II)-Sulfid
- Mit Nichtmetallen wie Phosphor oder Kohlenstoff erhitzt: Bildung von Phosphiden oder Carbiden
- Pyrophores Eisen, das fein verteilt ist, reagiert schon bei Raumtemperatur heftig an der Luft mit dem Sauerstoff. Es findet eine hohe Energiefreisetzung statt, wodurch es anfangen kann zu brennen oder glühen
Eisenverbindungen:
• Eisen(II)-Oxid, Eisen(III)-Oxid, Eisen(II,III)-Oxid
• Eisen(II)- Carbonat
• Eisen(II)-Sulfat
• Eisen(II)-Sulfid
• Eisen(II)-Hydroxid, Eisen(II)-Hydroxid
• Eisen(II)-Chlorid
Reaktionen von Eisen
• Fe + S --> FeS
• 2Fe + O2 --> 2FeO
• 2Al + Fe2O3 --> Al2O3 + 2Fe
• 2Fe2O3 + 3C --> 4Fe + 3CO2
Verwendung von Eisen
- Eisen gehört zu den meistverwendeten Metallen. Landfahrzeuge und Schiffe werden aus Eisen hergestellt. Im gesamten Baubereich wird es ebenfalls verwendet. Die häufigsten Metalllegierungen sind Eisen-Silicium, Eisen-Aluminium, Eisen-Nickel und Eisen-Kobalt. In der Chemie wird häufig reines Eisenpulver benötigt. Wenn man Gusseisen und Stahl herstellt, ist Roheisen ein Zwischenprodukt.
- Betrachtet man den prozentualen Gewichtsanteil an genutzen Metallen weltweit, so ist Eisen mit 95% das meist genutzte Metall.
- Da es in großen Mengen verfügbar ist, ist es recht preiswert und durch die hervorragende Festigkeit und Zähigkeit als Bestandteil von Legierungen ist es in vielen technischen Bereichen ein Grundwerkstoff (Fahrzeuge, Schiffe und Baubereich(z.B. Stahlbeton)).
- Da Eisen ferromagnetisch ist, wird es bevorzugt in Generatoren, Transformatoren, Drosseln, Relais und Elektromotoren als tragendes Bauteil des Elektromagnetismus verbaut.
- In Form einer Legierung mit anderen Metallen dient es als weichmagnetisches Material zur Führung, Abschirmung oder Erhöhung der Induktivität von Magnetfeldern.
- Eisen wird in den folgenden Formen verwendet:
- Roheisen enthält 4-5% Kohlenstoff und verschiedene anderen Elemente (Schwefel, Phosphor und Silicium). Es ist ein Vorprodukt in der Herstellung von Stahl und Gusseisen.
- Gusseisen enthält zwischen 2,06% und 6,67% Kohlenstoff und weitere Legierungselemente. Es gibt weißes und graues Gusseisen. Diese Unterscheidung findet im Vorkommen des Kohlenstoffes statt. Bei Ersterem kommt er als Carbid und bei letzterem als Graphit vor.
Da Gusseisen sehr hart uns spröde ist lässt es sich in der Regel nicht plastisch verformen. - Stahl enthält zwischen 0,06% und 2,06% Kohlenstoff. Er ist plastisch umformbar und kann durch legieren bzw. thermische Behandlung in seinen mechanischen Eigenschaften verändert werden.
- In der Medizin kann Eisen als Präparat eingesetzt werden um den Hämoglobinwert im Blut zu steigern.
Youtubevideos zum Thema Eisen und Stahl:
