Chemie
- Details
- Zugriffe: 30750
Name: Philipp Dietl, 2012
Fabian Müller, 2023-03
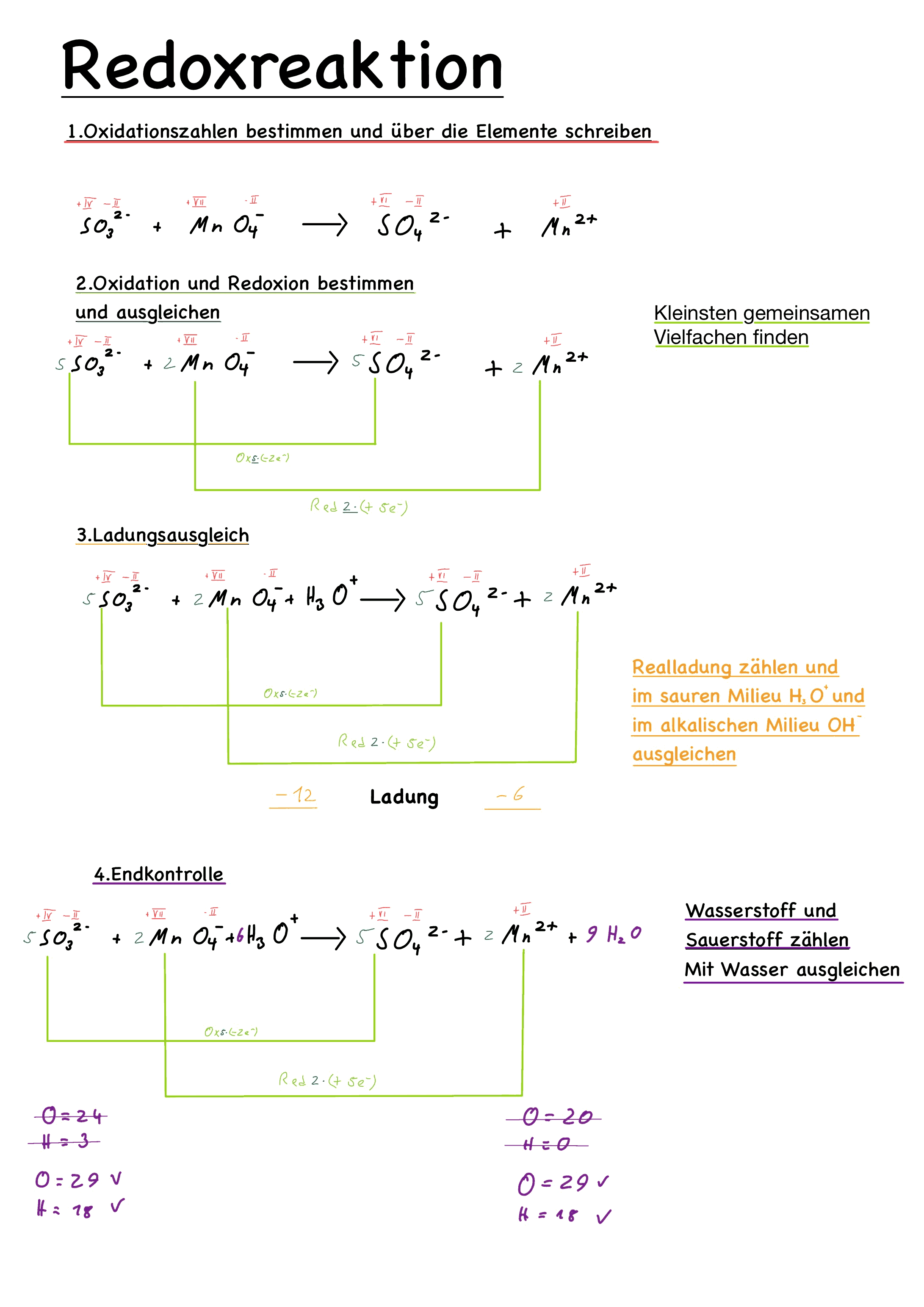
Grundsätzlich gibt es zwei Methoden, um komplexe Redoxreaktionen aufzustellen. Den vollständigen Weg oder die so genannte "Lasso"-Methode. Letztere geht unter Umständen etwas schneller. Diese Methode wird am Ende des Artikels erklärt.
1. Der vollständige Weg zum Erstellen von Redoxreaktionsgleichungen
Schritte zum Erstellen von Redoxgleichungen
1. Vorläufige Gleichung notieren ( in eckigen Klammern )
Man stellt Produkte und Edukte auf.
[Cu + HNO3 ---> NO2 + CuO ]
2. Oxidationszahlen ermitteln
Man bestimmt die Teilladungen aller Ionen und schreibt sie (mit Bleistift) oben drüber.
Cu: 0 ---> Cu: II Oxidation
H: -I ---> H: -I keine Reaktion
N: VI ---> N: IV Reduktion
O: -II ---> O: -II keine Reaktion
3. Teilgleichungen aufstellen
Red: HNO3 + e- ---> NO2
Ox: Cu ---> CuO + 2e-
4. Ladungsausgleich (mit H+/H3O+ und (OH)-)
Falls die Ladung auf der Linken Seite negativer ist als auf der Rechten Seite ergäntzt man entweder auf der Linken Seite H+/H3O+ oder auf der Rechten Seite (OH)-. Man ergäntz allerding nur soviele H+/H3O+/OH- wie unterschiedliche Ladung vorhanden ist. In alkalischer Lösung wird mit (OH)-(Hydroxidionen) und in in saurer Lösung durch H3O+/H+ (Oxioniumionen).
Red: HNO3 + e- + H+---> NO2
Ox: Cu ---> CuO + 2e- +2H+
5. Stoffausgleich mit Wasser
Nach dem man die Ladung ausgeglichen hat muss nun wieder der Stoffausgleich vorgenommen werden. Man gleicht mit H2O aus.
Red: HNO3 + e- + H+---> NO2 + H2O
Ox: Cu + H2O ---> CuO + 2e- +2H+
6. Elektronen Zahl durch Multiplikation untereinander ausgleichen
Man multipliziert beide, damit sie auf die selben Elektronenzahlen kommen.
Red: HNO3 + e- + H+---> NO2 + H2O |*2
Ox: Cu + H2O ---> CuO + 2e- +2H+ |*1
---------------------------------------------------------
Red: 2HNO3 + 2e- + 2H+---> 2NO2 + 2H2O
Ox: Cu + H2O ---> CuO + 2e- +2H+
7. Teilgleichungen addieren
Man addiert die beiden Teilgleichungen.
Red: 2HNO3 + 2e- + 2H+---> 2NO2 + 2H2O
Ox: Cu + H2O ---> CuO + 2e- +2H+
---------------------------------------------------------
Redox: 2HNO3 + 2e- + 2H+ + Cu + H2O ---> 2NO2 + 2H2O + CuO +2e- + 2H+
8. "Kürzen"
Man "kürzt" die Elektronen auf beiden Seiten. Falls vorhanden können auch Wassermoleküle und Wasserstoffionen gekürzt werden. Mathematisch ist es übrigens kein Kürzen, sondern eine Subtraktion.
Redox: 2HNO3 + Cu ---> 2NO2 + H2O + CuO
9. Bei Ionen wieder zu Salzen ergänzen
Falls die Ausgangsstoffen Verbindungen sind, in denen nur ein Teil von ihnen reagiert, so können diese Stoffe wieder in der Schluss Gleichung zusammengesetzt werden. Dieser Schritt ist allerdings nicht unbedingt notwendig.
10. Probe
Zum Schluss sollte man noch eine Probe machen. Man zählt die Ionen auf der Rechten Seite, den Edukten und auf der Linken Seiten, den Produkten.
H: 2/2
O: 6/6
N: 2/2
Cu: 1/1
Oxidation und Reduktion - Definitionen
Oxidation: Elektronenabgabe (Oxidationszahl wird größer )
Reduktionsmittel → Produkt + e-
Reduktion: Elektronenaufnahme ( Oxidationszahl wird kleiner)
Oxidationsmittel + e- → Produkt
2. Die "Lasso-Methode" zum Erstellen von Redoxreaktionen
Aufstellen von Redoxreaktionen nach der Lasso-Methode: Beispiel der anorganischen Chemie
- Anorganische Chemie: Redoxreaktionen im Alltag
- Anorganische Chemie: Salpetersäure HNO₃ - Herstellung, Verwendung, Eigenschaften
- Anorganische Chemie: Salpetrige Säure
- Anorganische Chemie: Salze
- Anorganische Chemie: Salzherstellung durch Neutralisation
- Anorganische Chemie: Sauerstoff
- Anorganische Chemie: Sauerstoffsäuren des Chlors
- Anorganische Chemie: Sauerstoffsäuren des Phosphors
- Anorganische Chemie: Säure-Base Chemie (Brönsted-Definitionen)
- Anorganische Chemie: Säure-Base-Puffer und Puffersysteme
- Anorganische Chemie: Säurestärke (pKs) und Basenstärke (pKb)
- Anorganische Chemie: Schwefel
- Anorganische Chemie: Schwefelsäure
- Anorganische Chemie: Stickstoff
- Anorganische Chemie: Struktur von Salzen, Ionengitter und Ionenbildung
- Anorganische Chemie: Übungsaugaben zum Massenwirkungsgesetz (MWG)
- Anorganische Chemie: Vergleich von Ionenbindung und Atombindung
- Anorganische Chemie: Wasserstoff
- Anorganische Chemie: Wie berechnet man Neutralistionsaufgaben (Beispielaufgaben)
- Anorganische Chemie: Wie funktioniert der Lithium-Ionen-Akku?
- Anorganische Chemie: Zink
- Anorgansiche Chemie: Redoxreaktion - Beispielaufgaben
- Biochemie: Biokatalysatoren (Enzyme)
- Chemie: Oxidationszahlen und deren Bestimmung (!)
- Farbigkeit und Molekülstruktur
- Glossar: Fachbegriffe der anorganischen und organischen Chemie mit Erklärungen
- Komplexchemie: Anwendungen der Komplexchemie
- Komplexchemie: Aquakomplexe
- Komplexchemie: Aufbau von Komplexen
- Komplexchemie: Chelatkomplexe
- Komplexchemie: Historischer Abriss der Entdeckung der Komplexchemie
- Komplexchemie: In der Natur vorkommende (biologische) Komplexverbindungen
- Komplexchemie: Komplexe Gleichgewichtsreaktionen und die Stabilitätskonstanten
- Komplexchemie: Komplexstabilitätskonstante und Komplexzerfallskonstante
- Komplexchemie: Ligandenaustauschreaktionen
- Komplexchemie: Nomenklatur (Benennung) von Komplexen
- Komplexchemie: Wasserenthärtung
- Ökologische, ökonomische und soziale Nachhaltigkeit in Chemie
- Organische Chemie: Gelatine
- Selektivität und Spezifität von Katalysatoren
- Herstellung von Maßlösungen
- I-Effekte beeinflussen die Säurestarke von Carbonsäuren
- Organische Chemie: Oxidative Fettumwandlung (Ranzigwerden von Fetten)
- Organische Chemie: Alkane - feste Alkane // Wachse und Paraffine
- Organische Chemie: Alkane - flüssige Alkane
- Organische Chemie: Alkane - gasförmige Alkane
- Organische Chemie: Alkanole (Alkohole)
- Organische Chemie: Alkene und Alkine
- Organische Chemie: Alkohol und seine Wirkung auf Menschen
- Organische Chemie: Alkoholate
- Organische Chemie: Alkohole: Ethanolherstellung durch alkoholische Gärung und großtechnische Produktion
- Organische Chemie: Aminosäuren - Peptidbindung, Typen, Aufbau, Reaktionen
- Organische Chemie: Anorganische Ester
- Organische Chemie: Aufgaben und Übungen zur Nomenklatur bei organischen Verbindungen
- Organische Chemie: Benzin und Diesel
- Organische Chemie: Bestimmung von Schmelz- und Siedepunkten
- Organische Chemie: Biogasanlagen
- Organische Chemie: Brennbarkeit von Kohlenwasserstoffen
- Organische Chemie: Carbonsäuren: homologe Reihe, Verwendung
- Organische Chemie: Carbonylverbindungen - Aldehyde
- Organische Chemie: Carbonylverbindungen - Ketone
- Organische Chemie: chemische Nachweise bei organischen Verbindungen
- Organische Chemie: Cis-/ trans-Isomerie und E/Z-Isomerie
- Organische Chemie: Cycloalkane und Cykloalkene
- Organische Chemie: Darstellungsweisen organischer Verbindungen
- Organische Chemie: Der Einfluss der I-Effekte auf die Säurestärke
- Organische Chemie: Die Aminosäure Glycin
- Organische Chemie: Die Chemie der "Shisha"
- Organische Chemie: Die Harnstoffsynthese von Friedrich Wöhler
- Organische Chemie: Eigenschaften von Aminosäuren
- Organische Chemie: Einfluss von Molekülmasse und Van der Waals-Kräften auf die Schmelz- und Siedepunkte
- Organische Chemie: Elektrophile und nukleophile Addition
- Organische Chemie: Eliminierung
- Organische Chemie: Energetische Betrachtung organischer Reaktionen
- Organische Chemie: Erdöl und Erdgas
- Organische Chemie: Erdöldestillation zur Gewinnung von Kohlenwasserstoffen
- Organische Chemie: Ester und die Veresterung
- Organische Chemie: Esterspaltung durch Hydrolyse
- Organische Chemie: Ethan
- Organische Chemie: Ethanol
- Organische Chemie: Ethen, Propen und Buten
- Organische Chemie: Ethin
- Organische Chemie: Ethin, Propin, Butin
- Organische Chemie: Färbeverfahren
- Organische Chemie: Fehlingprobe & Tollens-Probe
- Organische Chemie: Fehlingprobe und reduzierende Eigenschaften bei Kohlenhydraten
- Organische Chemie: Fette
- Organische Chemie: Fetthärtung und Margarineherstellung
- Organische Chemie: Fettsäuren
- Organische Chemie: Fischer-Projektion und die Umwandlung in die Haworth-Projektion
- Organische Chemie: Fluor-Chlor-Kohlenwasserstoffe (FCKW)
- Organische Chemie: Fruchtsäuren
- Organische Chemie: Fructose
- Organische Chemie: Galactose (!)
- Organische Chemie: Glucose (Traubenzucker)
- Organische Chemie: Glycogen (tierische Stärke)
- Organische Chemie: Glycosidische Bindung
- Organische Chemie: Gummi und Kautschuk
- Organische Chemie: Halogenalkane (!)
- Organische Chemie: Homologe Reihe der Alkane (!)
- Organische Chemie: I-Effekte
- Organische Chemie: Insulin
- Organische Chemie: Isobuten
- Organische Chemie: Isomaltose & Maltose als typische Disaccharide
- Organische Chemie: Isomerieformen
- Organische Chemie: Kerosin und Schweröl als Erdölbestandteile
- Organische Chemie: Keto-En(di)ol-Tautomerie bei Monosacchariden
- Organische Chemie: Kohle und Graphit
- Organische Chemie: Kohlenhydrate - Disaccharide
- Organische Chemie: Kunststoffe I - Allgemeines und radikalische Polymerisation
- Organische Chemie: Kunststoffe im Vergleich: Thermoplaste
- Organische Chemie: Lactose
- organische Chemie: Löslichkeit von organischen Verbindungen (polare und apolare Lösungsmittel)
- Organische Chemie: Mechanismus Veresterung
- Organische Chemie: mehrwertige Alkohole (Alkanole)
- Organische Chemie: Methan
- Organische Chemie: Nachweis von Proteinen (Ninhydrin-Reaktion)
- Organische Chemie: Nachweise für ungesättige Fettsäuren
- Organische Chemie: Nitril als wichtiger Kunststoff
- Organische Chemie: Nomenklatur und Benennung von organischen Kohlenwasserstoffen
- Organische Chemie: Nukleophile Addition
- Organische Chemie: Nukleophile Substitution
- Organische Chemie: Optische Aktivität
- Organische Chemie: Oxidation und Reduktion von Aldehyden
- Organische Chemie: Oxidation von Alkoholen
- Organische Chemie: Oxidation von Glucose mit Methylenblau (blaues Wunder)
- Organische Chemie: Pektine
- Organische Chemie: Petrochemie
- Organische Chemie: Plexiglas als Kunststoff
- Organische Chemie: Polare und apolare Lösungsmittel und Lösungmitteleigenschaften (!)
- Organische Chemie: Polykondensation von Nylon
- Organische Chemie: Polysaccharide
- Organische Chemie: Propan
- Organische Chemie: Radikalische Substitution
- Organische Chemie: Reaktionsmechanismen der organischen Chemie (Übersicht)
- Organische Chemie: Redoxreaktionen und Oxidationszahlen bei organischen Verbindungen
- Organische Chemie: Saccharose
- Organische Chemie: Schmelz- und Siedebereiche von Fetten und Ölen
- Organische Chemie: Schmelz- und Siedepunkte von Alkanen und Alkenen
- Organische Chemie: Schmerzmittel
- Organische Chemie: Spiegelbildisomerie (Stereoisomerie)
- Organische Chemie: Stärke (Amylose und Amylopektin)
- Organische Chemie: Struktur- und Eigenschaftsbeziehungen bei organischen Kohlenwasserstoffen
- Organische Chemie: Tenside
- Organische Chemie: Titration von Glycin
- Organische Chemie: Typen von Carbonsäuren
- Organische Chemie: Verbrennung von Alkanen und CO2-Emission
- Organische Chemie: Vergleich von Siedepunkten bei Alkanen, Alkanolen, Aldehyden und Carbonsäuren
- Organische Chemie: Verseifung
- Organische Chemie: Viskosität
- Organische Chemie: Was ist Organische Chemie?
- Organische Chemie: Zusammensetzung von Waschmitteln
- Organische Chemie: Zusammensetzung von Waschmitteln und deren Funktion
- Organische Chemie: Zwischenmolekulare Kräfte und Anziehungskräfte zwischen Molekülen
- Physikalische Chemie: Die Grundlagen der Thermodynamik